过敏性疾病是一个持续存在的临床挑战,治疗选择有限。因此,找到一种治疗过敏原的方法、改善过敏性疾病的技术尤为重要。
2022年1月17日,美国INDOOR生物技术公司的研究团队在《Frontiersin Allergy》杂志上发表了一篇题为 New Frontiers: Precise Editing ofAllergen Genes Using CRISPR 的文章,该文章表示,基因组工程,特别是CRISPR编辑,提供了从源头有效删除过敏原基因的可能性,这可能会极大地造福过敏个体。
迄今为止,CRISPR已经在一些治疗性应用中显示出前景,这无疑将指导疾病管理和治疗的新方法的发展。例如,CRISPR-Cas9被用来删除CEP290基因的突变,该基因是导致Leber先天性失明10型(LCA10)的原因,这是一种严重的视网膜营养不良症,通常源于单点突变引起的异常剪接。
镰状细胞病(SCD)和输血依赖性β-地中海贫血(TBT)是血红蛋白β亚单位基因(HBB)突变导致的红细胞异常或不足的两种情况,也是用CRISPR-Cas9的目标。
上述应用强调了CRISPR技术在解决单基因疾病方面的价值,特别是那些有相对简单的方法提供治疗的疾病(如直接视网膜下注射或体外血细胞编辑)。然而,许多CRISPR应用将需要对相关细胞或组织进行原位编辑,这最终将需要更复杂的递送方法或载体。目前,体内传递主要限于使用病毒载体或脂质纳米颗粒。
最近,CRISPR技术被用来在体外敲除Fel d 1的基因。从50只家猫的组织样本中提取基因组DNA,并对CH1和CH2进行测序,以确定基因中适合用CRISPR技术靶向的保守区域。评估了10个针对Fel d 1链1或2的sgRNA的小组。每个CRISPR sgRNAs与Cas9核酸酶一起使用脂质转染法传递到永生的猫科动物肾上皮细胞。通过对每个sgRNA的DNA序列分解或T7E1错配检测来评估CRISPR诱导的帧移突变导致的Fel d 1基因敲除。
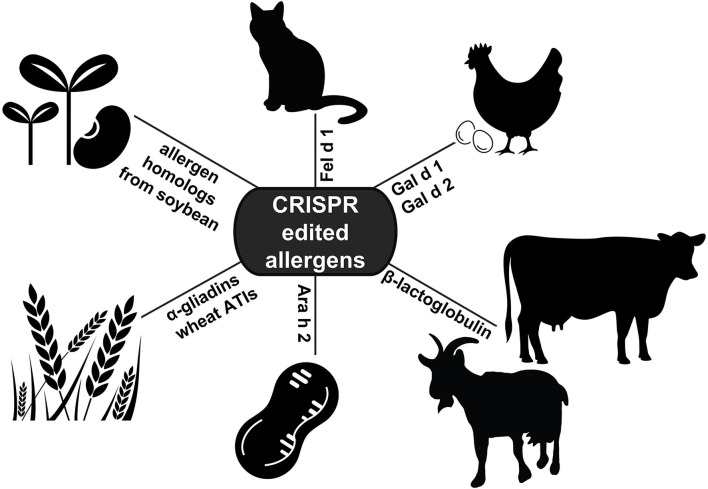
迄今为止,CRISPR技术除了编辑猫的过敏原基因,还可编辑母鸡蛋、大豆、小麦、花生以及牛奶和山羊奶中的过敏原基因(ATI:α-淀粉酶/胰蛋白酶抑制剂)(如上图)。这些研究证明了该技术在提高我们对过敏原蛋白的理解方面的价值,并强调了CRISPR编辑在为过敏性疾病提供更好的替代治疗方案方面的巨大潜力。未来,CRISPR技术也可用于识别新型过敏原,或直接修改免疫反应,作为防止识别过敏原蛋白的一种方法。今后,对过敏原蛋白序列、结构或抗体结合位点的全面分析,对于识别基本功能域或保守序列,以CRISPR删除为目标,将是非常宝贵的。此外,进一步开发将CRISPR试剂有针对性地输送到体内特定细胞或组织的方法,将证明对成功编辑成年动物的过敏原基因至关重要。
CRISPR是现在应用比较成熟的基因编辑方法,但是操作比较复杂。用于基因的减弱/增强/编辑比较先进的方法是动物体内转染方法,有很多文章报道,方法简单,易于操作,最快3天可以得到结果。
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享