跑过琼脂糖凝胶电泳的小伙伴,是不是经常遇到过电泳拖尾的现象啊?相信不少人点头如捣蒜了。提个质粒拖尾,提个DNA拖尾,连PCR也拖尾,拖尾什么的最常见了。验证也就算了,关键是图片拍出来不好看了,发文章什么的太影响档次了。下面我就跟据自己的经验跟大家讲讲琼脂糖凝胶电泳为什么会拖尾,有不足的希望大家多多评论补足啊(三人行必有我师嘛)!!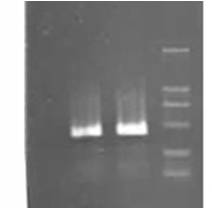
那琼脂糖凝胶电泳为什么会拖尾呢?
1. PCR产物出现拖尾的因素有很多,总结为一条,就是非特异性扩增过多。原因可能是:
(1) 模板不纯:纯化模板
(2) Buffer不合适:更换Buffer
(3) 退火温度偏低:适当提高退火温度
(4) 酶量过多:适量用酶,或调换另一种酶
(5) dNTP、Mg2+浓度偏高:适当降低dNTP和镁离子的浓度
(6) 循环次数过多:减少循环次数
(7) 模板量少或引物量过多:增加模板量,减少引物的用量
2. 提质粒的时候经常有这种个现象,有可能是样品浓度过高了。这种情况简单,稀释一下就行了。
3. 提基因组DNA的时候也常出现拖尾,最可能的就是提的DNA中掺杂有蛋白质,蛋白质会拽DNA的泳动。所以一定要注意提取基因的操作,减少蛋白质等杂质的出现。
4. 样品破碎或是被降解
5. 存在RNA:DNA前面的一片一般都是未清除的RNA,经过纯化,RNAse处理,就没有了
6. 电泳体系的问题:观察你的marker是否也存在拖尾现象,作为对照
(1)电泳缓冲液TAE或者TBE的污染:。建议更换缓冲液。
(2)上样时样品漂了,建议增加上样缓冲液的用量,以及小心加样。
(3)电压太高:适当降低电压
(4)根据核酸片断大小,适当把加大凝胶浓度。凝胶浓度的选择取决于DNA分子的大小。分离小于0.5kb 的DNA片段所需胶浓度是1.2-1.5%, 分离大于10kb的DNA分子所需胶浓度为0.3-0.7%, DNA片段大小间于两者之间则所需胶浓度为0.8-1.0%。
扫描右侧二维码,关注英格恩公众号,随时阅读沟通。
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享
