已有众多的文献报道,脂质体本身会参与细胞生理活动,引起基因表达的上调或下调。如参与PKC(蛋白激酶C)通路调节(Biochemistry.1992 Sep 22;31(37): 9025-30);如抑制ATP酶的活性(Biochim Biophys Acta.2008 Apr;1777(4):362-8);如与线粒体膜发生作用(J Biol Chem. 19 …
阅读更多 »RNA转染(entranster)后沉默现象不明显怎么办?
可能原因: 1. RNA与转染试剂比例不佳。可进行预实验优化。 2. 细胞密度不佳。 调整细胞密度到转染时汇合度为20-40%。 3. RNA效率不高。选择最优RNA,并采用已知高效的RNA做对照。 4. RNA酶污染。建议无RNA酶和内毒素的吸头、离心管和溶液等材料和实验器具。 5. 转染后培养时间不够。在mRNA水平可以到48 小时以后验证结果,在蛋白水 …
阅读更多 »体外培养细胞的一般性质(五)
体外培养细胞传代规范的建立 细胞从原代培养时开始,就要建立细胞传代常规,即最好依据严格的时间表进行传代等操作,这样可以保持和监控细胞的增殖行为。若到了适合的时间,细胞还没有达到足够高的密度(即细胞没有彼此汇合),那么应增加接种密度:相反,若细胞很快彼此汇合,则应降低接种密度。理想的细胞浓度是使细胞每3~4d 更换培养液,每7d 传代。常规传代使细胞可重复标准 …
阅读更多 »已经把miRNA转染到了SW480细胞中,用来抑制RUNX1的表达,从而抑制细胞行为。已经通过WB验证了转染三天后RUNX1受到了抑制。现在的问题是应该在转染三天后消化细胞再做划痕实验,还是先种板做划痕再进行转染。
我的建议: 通常来说,如果你想研究miRNA对划痕愈合(细胞迁移)的影响,建议先进行miRNA转染,等待足够的时间让miRNA发挥作用(你提到的是三天),然后再进行划痕实验。这可以确保在进行划痕实验时,RUNX1已经被下调,迁移实验所观察到的结果是由RUNX1抑制所导致的。 但如果你担心转染后细胞的粘附性不好或者转染效率不高,也可以先进行划痕实验,让细胞在板 …
阅读更多 »细菌生长曲线的测定及其意义
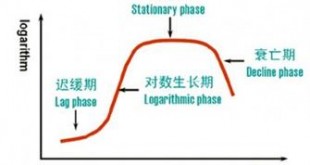
细菌生长曲线,就是将少量细菌接种到一定体积的、适合的新鲜培养基中,在适宜的条件下进行培养,定时测定培养液中的菌量,以菌量的对数作纵坐标,生长时间作横坐标,绘制曲线。 一、 细菌生长曲线的测定方法 1、菌种培养:取大肠杆菌斜面菌种1支,以无菌操作挑取1环菌苔,接入肉膏 蛋白胨培养液(LB)中,静止培养12–14h,备用。 2、制备LB培养基100m …
阅读更多 »siRNA是从牵牛花过表达发现的吗
siRNA(small interfering RNA, 小干扰RNA)并不是从牵牛花的过表达现象中发现的,而是从研究植物基因沉默和RNA干扰现象中逐步发展起来的。siRNA的发现归功于对基因沉默和RNA干扰机制的研究,尤其是科学家在植物、真菌和线虫等生物中对这些现象的观察和研究。 siRNA发现的关键研究 植物基因沉默:在植物中,科学家观察到特定基因可以在 …
阅读更多 »我自己订的shRNA的质粒,不管是瞬转还是稳转,转录水平敲下来了百分之90了,但是蛋白水平就是不变😰。48小时、96小时、120小时我都收过,都是这样。我该怎么办呢?
根据描述,您的shRNA已经成功将转录水平(mRNA水平)敲低了90%,但蛋白水平却没有显著变化。这种情况在RNA干扰实验中并不罕见,可能由以下原因导致: 可能原因分析 蛋白半衰期较长: 有些蛋白具有较长的半衰期,即使mRNA水平显著下降,蛋白水平可能仍然稳定。这是因为已有的蛋白质分子不会立即降解,需要更长时间才能逐渐减少。 翻译后调控: 某些蛋白质可能受翻 …
阅读更多 »怎样提高细胞转染效率?
1.选择合适的转染试剂 不同细胞系转染效率通常不同,但细胞系的选择通常是根据实验的需要,因此在转染实验前应根据实验要求和细胞特性选择适合的转染试剂。每种转染试剂都会提供一些已经成功转染的细胞株列表和文献,通过这些资料可选择最适合实验设计的转染试剂。当然,最适合的是高效、低毒、方便、廉价的转染试剂。如英格恩的 …
阅读更多 »电转效率受哪些因素影响?
电穿孔效率受以下几种因素的影响: 外加电场的强度。电压过低,培养细胞质膜的改变不足以允许DNA 通过; 电压过高,细胞会受到不可逆的损伤。对于大多数哺乳动物细胞系, 电压250~ 500V/cm时可达到最高瞬时表达水平。通常经过电穿孔, 20% ~ 50%的细胞能够存活(根据台盼蓝拒染法的检测结果) ( Patterson 1979; Baum et al. …
阅读更多 »TUNEL分析
TUNEL方法(末端脱氧核苷酸转移酶介导的dUTP-地高辛配基切口标记)源自完整固定的细胞核DNA 裂解部位标记(如Gavrieli et al. 1992)。 该法可用于组织切片、玻片上细胞生长、流式细胞计量术分析,用于组织切片的改进程序由Naik 及其合作者提出(Naik et al. 1996) ,叙述如下 1、组织切片的TUNEL 染色1)取下组织, …
阅读更多 » 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享