长链dsRNA 的导入能够在小鼠卵母细胞、早期胚胎、胚胎干细胞和胚胎癌细胞( Svoboda et al. 2000; Wianny and Zemicka-Goetz 2000; Billy et al. 2001; Yang et al. 2001),以及植物、蠕虫、果蝇体内诱导特定和高效的RNA 干扰。但是,早期在哺乳动物体细胞中用长链dsRNA 诱导RNA 干扰的尝试未能成功,因为长链dsRNA 作为一个前体会诱导干扰素反应。这种通常被视为毒感染反应的天然免疫反应能够诱导RNA 的非特异性降解以及广泛抑制蛋白质生物合成,最终导致细胞凋亡。使用3′ 端带有2 个非配对碱基的2 1 ~ 23个核昔酸的双链siRNA, 即一种RNA 干扰信号通路的中间体,能模拟长链dsRNA 经Dicer酶切割后的自然产物可以克服这一障碍(Caplen et al. 200 1; Elbashir et al.2001,2002) 。后续研究表明,内源性表达的siRNA 和shRNA 引起靶基因特异性抑制的效率与转染外源性siRNA 相当。
siRNA 设计
最初, siRNA 序列的选择是基于实验经验而获得的(Elbash订et al. 2001 , 2002) 。最近,生物信息学工具被用来设计siRNA (表1,见文章 应用长链dsRNA 抑制基因表达 ) ,目前多个数据库收录了经过实验确证的siRNA 和shRNA 。值得推荐的是,在设计新的siRNA 之前可以通过搜索已有的siRNA 数据库和科研文献来寻找已确证的siRNA 。如果不能获得已确证的siRNA, 则应该为每个靶基因设计3 ~ 5 条候选siRNA ( Pei and Tuschl 2006 ) 。以下将介绍如何挑选有效和特异性
强的siRNA 。
- 目标区域。siRNA 通常以mRNA 的CDS 序列为靶点,因为一般认为,相对非编码序列而言, CDS 序列容易成为RNA 干扰的靶点且多态性更低。然而,当CDS 不容易找到合适的siRNA 结合位点,或者为了区分两个编码区相同但3’非翻译区(UTR )不同的基因时, 3 '端UTR 也可以利用。5 端UTR 和剪接点通常不被考虑,因为它们可能会被细胞内蛋白质复合体(如翻译起始机器或者外显子连接复合体)所包裹。
- 长度和非配对结构。尽管20 ~ 25 个核苷酸长度、包含2 个非配对碱基形成的3’端突出“尾巴"的双链siRNA 显示出了与常规siRNA 相当的效率,但常规的双链siRNA依然是长度为21 个核苷酸、两端包含2 个非配对碱基形成的3′ 端突出“尾巴",模拟了Dicer 酶体内切割的主要产物。长度超过3 0 个碱基的双链RNA 能够在哺乳动物体细胞中诱导干扰素反应。一些长度超过23 个碱基的RNA 双链体能够诱导细胞特异性的于扰素反应(Reynolds et al. 2006) 。
- 热力学不对称性。进入RISC 的siRNA 链被称为“向导链" 。这一siRNA链的5′ 端碱基配对较为松弛(动力学稳定性稍差),被RNA 干扰机器识别为向导(Khvorova et al. 2003 ; Schwarz et al. 2003 ) 。向导链进入RISC, 两者之间的这种结合会通过5’端的G:U 错配得到加强。反之, 也可以通过化学修饰减弱信使链(向导链的反义链,目标mRNA 的同义链)与RISC 的结合(Nykanen et al. 2001; Chen et al. 2008).
- GC 含量和核苷酸偏好。有关siRNA 设计的大量分析显示: 具有生物学功能的siRNA不能含有回文( palindromic ) 序列和内在重复序列,并且GC 含量达到3 0% ~ 52% 。回文序列或者内在重复序列会形成二级结构,干扰与RISC 以及目标mRNA 的结合( Patzel et al. 2005) 。GC 含量过高或者过低会干扰两条siRNA 链的分离,减慢与RISC的结合。此外,成熟RISC 与目标mRNA 的强烈结合会妨碍切割产物的释放,使酶的转换效率降低( Haley and Zamore 2004; Tang and Zamore 20 04 ) 。有关高效siRNA性质的多因素分析显示: 向导链的第1 ~第7 个碱基应该是U 或者A, 第10 个碱基应为A 或者U, 第19 个碱基应为G 或者C (Pei and Tuschl 2006 ) 。这些“规律”预示了向导链的结合喜好,使其与靶标保待适当的亲和力,促进对靶标的多轮切割。
- RNA 干扰介导的脱靶效应。RNA 干扰介导的脱靶效应是指双链siRNA 的向导链或信使链介导的对基因表达的非特异性抑制,具有浓度依赖性(图1) Oackson et al 2006a ) 。RNA 干扰介导的脱靶效应通常会在siRNA 发挥类似内源性mRNA 的作用时发生,即通过小RNA 向导链的“种子序列”(2~7 位或2~8 位核昔酸)与其目标mRNA 结合(Lim et al. 2005; Lin et al. 2005; Bilmingham et al. 2006) 。目前已经有多种消除这种脱靶效应的方法。尽管通过同源性搜索(如BLASTn 或者 Smith-Wate1man 算法)来减少可能存在脱靶效应的s戊NA 的方法应用比较广泛,但这一方法仍不能消除大多数的脱靶效应,这是因为无法避免第6 位和第7 位核苷酸与细胞内mRNA匹配的偶然情况。通过将针对同一 mRNA 的多个无相关性siRNA混合使用以降低每一种siRNA 浓度的方法可提高RNA 干扰的特异性(知ttler et al 2007) ,但是这种方法有着严格的适用要求。对siRNA 向导链的第2 位核苷酸进行不依赖于序列的化学修饰同样可以提高效率,这一方法减少了siRNA 对既定靶标以
及靶标之外mRNA 的亲和力(Jackson et al. 2006b) 。唯一被证实的可提高RNA 干扰特异性的方法是设计siRNA 分子,使其正确的RNA 链进入有功能的RNAi 酶复合体,或者可以对信使链进行化学修饰,以阻止其通过RNA 干扰途径发挥作用( Elm的et al. 2005) 。
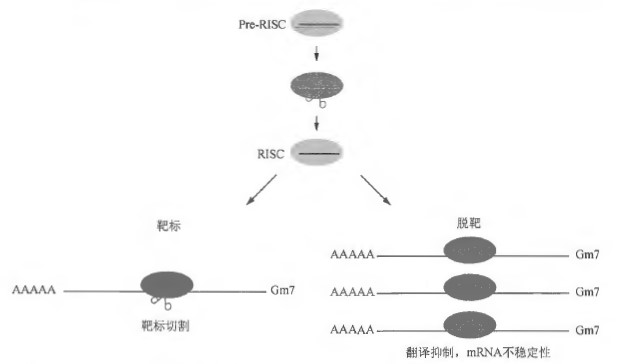
行切割,即通常所说的RNA 干扰过程。但是, siRNA 也可以发挥类似细胞内miRNA 的作用,即通过部分碱基配对与其RNA 靶标相匹配。这种miRNA 的作用偶尔会导致对非靶标m阳寸A 的抑制作用,即脱靶效应。
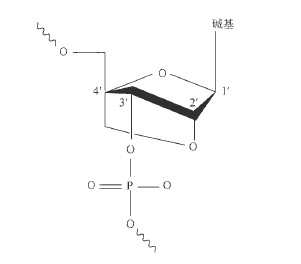
天然免疫反应和毒性。在哺乳动物中,如果siRNA 包含富含G 和U 的序列基序,如GUCCUUCAA 或者UGUGU, 那么此siRNA 有可能通过Toll 样受体激活细胞内的天然免疫通路(Hornung et al. 2005; Judge et al. 2005; Marques and Wil-liams 2005;Sioud 2005) 。然而,其他的免疫刺激因素仍然有待鉴定,因为有一些siRNA 虽富含G 和U 却不能激活免疫受体,而另一些缺少GUCCUUCAA 或者UGUGU 基序的siRNA 反而具有免疫刺激活性。针对176 个随机挑选的siRNA 进行比较研究,鉴定出UGGC 是一个毒性基序,能引发细胞死亡(Fedorov et al. 2006) 。已知的免疫刺激活性和毒性基序可以通过计算预测而避免。另外,化学修饰,如锁状核酸Clocked nucleic acid, LNA) (图2) 和对免疫刺激活性和毒性基序进行2′-O– 甲基化核酸修饰可以用于抑制其天然免疫刺激活性(Judge et al. 2006) 。
siRNA 的体外制备
化学合成siRNA 。合成siRNA 应用广泛,这种方法的得率和纯度都比较高。对合成siRNA 还可以进行一系列化学修饰以提高siRNA 的稳定性、降低脱靶效应,以及(或者)阻止激活天然免疫反应。
利用酶学反应从长链dsRNA 生成siRNA 。利用重组Dicer 酶或者细菌RNaseⅢ 对体外转录获得的长链dsRNA 进行酶学消化也可以获得双链siRNA ( Yang et al 2002) 。与合成siRNA 相比,对长链dsRNA 酶消化可以生成不同种类的siRNA,提高了生成功能性siRNA 的可能性。然而,体外酶学反应生成siRNA 的主要不足之处在于:这些siRNA 在使用时不易选择对照。理论上,对照siRNA 不应该与实验siRNA 具备相同的种子序列。由千体外酶切生成的确切siRNA 无从得知,那么
也就无法选择精确的对照,因此,无法区分究竟是既定靶标mRNA 还是脱靶基因的特定表型表达发生下调。
体外转录。利用合成的、含有噬菌体启动子的DNA 寡核苷酸模板,经体外转录可以生成siRNA 。通常,这一方法通过核酸酶或者核酶消化,确保产物拥有确定的末端以及(或者) 5 '端单磷酸或者经基末端。这一方式能够以较低成本快速生成多个不同siRNA ,但是风险主要存在于污染的三磷酸RNA 会触发天然免疫反应(Kim et al. 2004) 。
siRNA 、shRNA 和shRNAmir 的细胞内表达
在细胞内利用DNA 模板表达siRNA 、shRNA 和shRNAmir ( miRNA-adapted shRNA)能够诱导瞬时、持续或者可诱导的基因沉默,有助于对功能缺失表型进行系统分析。
基于DNA 的siRNA 表达。在基于DNA 的siRNA 表达方法中, siRNA 的有义链和反义链由同一质粒中不同的RNA 聚合酶III 启动子转录而成。转录后,有义链和反义链通过分子内配对形成双链siRNA 并触发RNA 干扰(Lee et al. 2002; Miyagishi and Taira 2002) 。两条siRNA 链在细胞核内的杂交有可能会由于向细胞质转运而无效; shRNA 以及类似策略已经取代上述方法。
shRNA 。shRNA 可以作为单链RNA 分子转录形成,与含有19 ~ 29 个核苷酸的" 茎”结构和4 ~ 15 个核昔酸“环”结构的前体rniRNA C pre-miRNA ) 类似。转录后,shRNA 由细胞核转运至细胞质, 在细胞质中,“环”结构被Dicer 酶切割产生siRNA( Castanotto et al. 2002; McManus et al. 2002; Paddison et al. 2002) 。有两种方法可用来表达shRNA : a. 基于PCR 的shRNA 表达盒( PCR-derived shRNA-expressioncassettes ): b. shRNA 表达质粒或病毒载体。基于PCR 的shRNA 表达盒可以避免克隆过程, 并且能够快速生成大量shRNA, 主要用于筛选功能性shRNA 。这一方式由于缺乏抗生素筛选标记而仅能瞬时诱导基因沉默。相反, shRNA 表达载体能够整合到基因组或者作为游离基因稳定地复制,既可以用于瞬时表达shRNA, 也可以用来建立转基因的RNA 干扰细胞系或动物,实现针对不同发育阶段和组织类型基因功能缺失的系统研究。
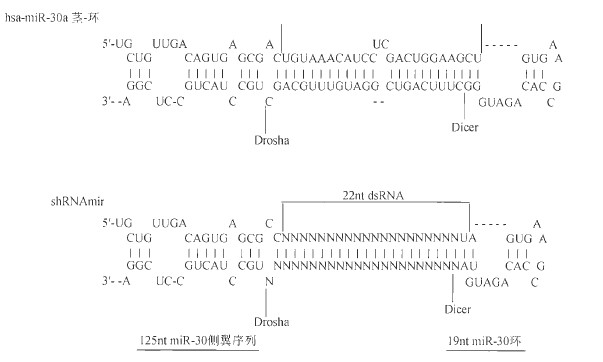
shRNAmir。 目前,通过将人pre-rniR-30 的茎序列替换为所需的siRNA 序列可以构建shRNArnir (图3) 。这样, siRNA 被植入天然pre-miRNA 之中,实现Drosha和Dicer 酶对siRNA 的有效切割, 最终促进siRNA 向导链与成熟RISC 的相互作用。与标准shRNA 相比, shRNAmir 能对靶标进行更高效的抑制(约提高12 倍)。因此,shRNArnir 被称为“第二代shRNA” (Zeng and Cullen 2002, 2003; Zeng et al. 2003;Silva et al. 2005) 。
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享