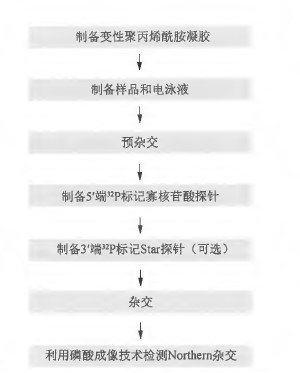
该方案描述如何运用Northern 杂交检测15~150 个核昔酸的小RNA (图1) 。通过聚丙烯酰胺凝胶电泳分离总RNA, 再采用半干法进行转膜。RNA 通过紫外线照射交联至尼龙膜上,在Church 缓冲液中对RNA 和α-32p标记的寡核昔酸探针进行杂交,并用磷酸成像分析技术(phosphorimager analysis) 进行检测分析。使用包含两个结构域的StarFire探针可以提高杂交探针的放射特性。StarFire 探针5′ 端的结构域可以特异性地与目标小RNA 杂交, 3 '端结构域可以与携带10 个脱氧胸腺嘧啶核苷的5′ 端寡聚核苷酸相互结合,从而在StarFire 探针的3′ 端形成可以与DNA 聚合酶相互结合的10 [α-32p] 脱氧腺苷。
试剂
丙烯酰胺:双丙烯酰胺(19 : 1, 40%, m/ V)
[ α-32p]dATP (6000Ci/mmol,10mCi/mL)
硫酸按(10%, m/ V)
Church 缓冲液
甲酰胺上样电泳缓冲液<A>
[γ-32P]ATP (6000Ci/mmol,≥ 10mCi/mL)
miRNA StarFire 核酸标记仪(DNA 合成技术)
StarFire 探针( 50 个核苷酸以上, 聚丙烯酰胺凝胶电泳纯化)
StarFire 通用模板(高效液相层析)
StarFire 10X 混合缓冲液( 100mmol/L Tris 7.5, 50mmol/L MgCl2, 75mmol/L DTT )
StarFire 终止缓冲液( 10mmol/L EDTA )
Exo- Klenow DNA 聚合酶
RNA 样品和5’端32P-放射性标记的RNA 分子质量标准
SDS (20%, m/V)
SSC (1 X, 20 X)
合成的寡核苷酸探针( DNA 、RNA 或LNA-modified DNA)
T4 多聚核苷酸酶( 10U/μL)
T4 多聚核苷酸酶缓冲液(10 X)
TBE 缓冲液( 5 X 和0.5X)
TE 缓冲液( pH 8.0 , 10 X 和1 X)
TEMED (四甲基乙二胺)
尿素
设备
印迹滤纸(加厚)、加热模块( 95 °C)、杂交箱、杂交管、磁力搅拌器、带正电荷尼龙膜、磷酸成像仪、磷酸成像板、聚丙烯酰胺凝胶装置、Saran 保鲜膜、半干法转膜设备
方法
制备变性聚丙烯酰胺凝胶
1.配制含8 mol/L 尿素的15 %变性聚丙烯酰胺凝胶
| TBE 缓冲液(5X) | 2mL |
| 丙烯酰胺:双丙烯酰胺( 19 : I, 40%, m/V) | 3.75mL |
| 尿素 | 4.8g |
| 去离子水 | 至10mL |
2 . 室温条件下用磁力搅拌器搅拌溶液至尿素完全溶解。
3 确定胶规格并组装配胶设备。
4 加入100μL10% ( m/ V) 的过硫酸按。
5 加入10μL (TEMED) 四甲基乙二胺。
6 快速混合溶液并灌胶,插10 孔梳子。室温下聚合20min 。
样品制备及电泳
7 将5 ~ 10μg 的总RNA 样品与上样缓冲液等体积混合, 终体积为10μL 。
8 95℃ 加热5min, 置冰上冷却。
9 冲洗胶孔除去尿素,保证条带一致且整齐, 然后上样10μL/孔,必须设立含10 X 5’端32P-放射性标记的RNA 标准。按照说明书,使用T4 聚核苷酸激酶和[γ-32P] ATP 对RNA分子质量标准进行标记,然后稀释200 倍, 使其适合小RNA 的杂交检测。
10 用0.5 X TBE 缓冲液200V 电泳约1h, 直至溴酚蓝至胶底部。
半干法RNA 转膜
11 根据胶大小,切一张带正电荷的尼龙膜和两张加厚印迹滤纸,并浸入0.5 X TBE 缓冲液中,室温浸泡10min 。
12 在铅阳极放一张预浸湿的印迹滤纸,并用塑料移液管排尽气泡。
13 在印迹滤纸的上面放一张提前浸湿的膜, 并排尽气泡。
14 小心地将胶转移至第一层膜上,并排尽气泡。
15 将另外一张提前浸湿的印迹滤纸放在胶上,并排尽气泡。
16 将阴极与胶膜组合( sandwich stack) 连接并盖上保护盖,恒压20V 转膜1h 。
17 转膜完成后,将湿膜放在一张滤纸上, 254nm 紫外线照射( Stratalinker; 120000μJ的自交联装置)交联RNA 至膜上。
18 将交联后的膜放入杂交管中, RNA 面向内。加入20mL Church 缓冲液,将杂交管放入杂交箱中孵育1h, 37℃ 旋转预杂交过夜。
制备5’端32p-放射性标记的寡核苷酸探针
19 相同长度的探针可以与小RNA 完全互补, 5’端标记反应所用试剂:
| 无核酸酶的水 | 6μL |
| DNA 寡核苷酸探针( 25μmol/L) | 1μL |
| T4 多核苷酸酶反应缓冲液(10X) | 1μL |
| T4 多核苷酸酶( 10 U/μL) | 1μL |
| γ-32P ATP ( 6000 Ci/mmol, ≥10mCi/mL) | 1μL |
20. 37°C 反应1h 。
21 根据使用说明书,用Sephadex G 25 旋转层析柱分离出未掺入的[γ-32P] ATP 。
制备3’端32P标记的StarFire 寡核苷酸探针(可选)
22 用1 X TE 缓冲液溶解StarFire 通用模板至浓度为12.5μmol/L 。
23 用1 X TE 缓冲液溶解StarFire 通用探针至浓度为100 μmol/L 。
24. 用无核酸酶的水将StarFire 通用探针稀释至0.5μmol/L 。
25 在0.5mL 的微量离心管中混合以下试剂:
StarFire 缓冲液( 10 X) 1μL
StarFire 探针( 0.5μmol/L ) 1μL
StarFire 通用模板(12.5μmol/L ) 1μL
26 . 用移液器将溶液混合,然后95°C 加热1min 。
27 取出试管冷却至室温(约5min) 。短暂离心并收集试管底部反应物。
28 加入6μL[α-32p] dATP ( 6000Ci/mmol, 10mCi/mL) 和1μL 的Exo-Klenow DNA 聚合酶,移液器轻吹混匀。
29 室温孵育2h, 加入40μL StarFire 反应终止缓冲液。
30 按照说明书,用Sephadex G25 旋转层析柱分离未掺入的[α-32p]dATP 。
杂交
31 预杂交后(步骤18 ) ,向预杂交溶液中加入5’端32p-放射性标记的探针或3’端32p-放射性标记的StarFire 探针,孵育2h 或者过夜。
32 杂交完成后,将杂交溶液小心转移到50mL 的锥形离心管中,-20℃ 储存。
33 用30mL 1 x SSC 和0.1% (m/V) SDS 混合液洗涤瓶子两次。
34 用30mL 1 X SSC 和0.1% (m/V) SDS 混合液37 °C 洗膜10min, 重复洗两次。
35 用Saran 保鲜膜封闭湿膜,并置于磷酸成像板上过夜。
36 磷酸成像仪读取杂交信号,并用相关软件对其进行分析。
不同样品小RNA 相对丰度分析
37 根据使用说明,用ImageGauge 软件对同一样品原始杂交信号和背景信号进行定量,并从原始信号中减去背景信号,即得到小RNA 特异杂交信号。
38. 500mL 0.1 % (m/V) SDS 煮膜10min,,从印迹中剥离( strip ) 出探针。用Saran 保鲜膜封闭湿膜,并将其置于磷酸成像板上过夜,从而检测探针剥离是否成功。若信号未完全消除,需重复此步骤。
39 将膜与内参特异性探针杂交(如样品中含有一个小核RNA 、tRNA 或5S 核糖体RNA ) , 如上所述,此方法可以检测各个样品内参的特异杂交信号。
40. 对目标小RNA 杂交信号通过内参特异性杂交信号进行标准化,不同样品的标准化值即可用于比较目标小RNA 的相对丰度。
样品中小RNA 绝对量分析
41 订购一种与目标小RNA 序列完全相同的RNA 寡核昔酸序列,并将其稀释成一系列浓度(10-1~103fmol) 。
42 将稀释的RNA 寡核苷酸和样品上样至变性聚丙酰胺凝胶,如上所述进行Northern杂交(步骤7~步骤36) 。
43 绘制RNA 寡核苷酸稀释样品浓度与特异杂交信号(确保减去背景)关系曲线,并对比两者的杂交信号从而得到标准曲线。根据标准曲线确定各个样品中小RNA 的绝对量。
疑难解答
问题( 步骤36 ) :没有检测到信号,但是检测到了5′ 端32p 放射性标记的分子质量标准。
解决方案: 尝试以下方法。
.检查探针序列是否与待检测目标小RNA 完全互补。
.将探针用15 %变性聚丙烯酰胺凝胶分离后,用磷酸成像仪检测探针是否标记完全。
.检查内参。
·为了提高灵敏度,用5′ 端32p 标记的RNA 寡核苷酸探针或者5′ 端32p标记的LNA修饰的DNA 寡核苷酸探针,将温度分别升高至60 °C 或70 °C 。
问题( 步骤36 ) :检测到背景杂交信号较高。
解决方案: 将预杂交延长至过夜。最后一次洗涤步骤重复两次或更多次。
配方
T4 多聚核苷酸激酶反应缓冲液( 1 0X)
| 试剂 | 体积(1mL ) | 终浓度( 10 X) |
| Tris-HCI ( 1mol, pH7.6) | 700μL | 700μmoL |
| MgCl2 ( 1mol ) | 100μL | 100μmoL |
| DTT ( 1mol ) | 50μL | 50μmoL |
| H2O | 150μL | |
| -20℃保存。 |
 英格恩生物技术博客 生物实验干货分享
英格恩生物技术博客 生物实验干货分享